El amoníaco es un compuesto químico con la fórmula NH3. El amoníaco, en disolución acuosa puede actuar como base,
agregando un átomo de hidrógeno y transformándose en el catión amonio NH4+.
El amoníaco es un gas incoloro, de olor característico por lo nauseabundo y penetrante. Se produce naturalmente en la descomposición de la materia orgánica, y también es producido a nivel industrial. A temperatura ambiente se disuelve fácilmente en agua y se evapora con rapidez.
El amoníaco es un gas incoloro, de olor característico por lo nauseabundo y penetrante. Se produce naturalmente en la descomposición de la materia orgánica, y también es producido a nivel industrial. A temperatura ambiente se disuelve fácilmente en agua y se evapora con rapidez.
El amoníaco es producido de manera natural por
bacterias que se encuentran en el suelo, y que degradan la materia orgánica
proveniente de desechos de animales, y plantas y animales muertos.
Una cantidad de amoníaco similar a la producida
naturalmente es obtenida anualmente de manera industrial. La mayor parte del
amoníaco obtenido de esta manera se destina a la producción de
fertilizantes. En menor proporción, se utiliza en producción de productos de
limpieza, refrigerantes, alimentos, bebidas entre otros.
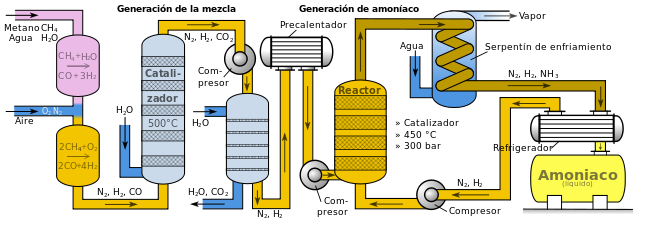
El proceso mediante el cual se obtiene amoníaco obtiene su nombre de los químicos que lo idearon: Fritz Haber y Carl Bosch. Este proceso es el resultado de la combinación directa entre el nitrógeno (proveniente de la atmósfera) y el hidrógeno (proveniente del gas natural), ambos en estado gaseoso:
N2(g) + 3H2(g) → 2NH3(g)
Esta reacción ocurre con lentitud, dado que necesita
gran cantidad de energía de activación, como consecuencia de la estabilidad
química del nitrógeno. Para acelerar la reacción se utiliza un
catalizador, y se aumenta la presión y la temperatura a la que esta
ocurre.
De esta manera las moléculas gaseosas tienen mayor
energía cinética, aumentando la velocidad con que reaccionan. Además, al
retirar el amoníaco a medida que se va formando, se acelera aún más la
producción del mismo.
La presión aplicada para mejorar el rendimiento de
esta reacción puede llegar hasta las 900 atmósferas. Con esta presión, a una
temperatura de 450 o 500 grados C, el rendimiento de la reacción puede ser del
40%.
El amoníaco obtenido de esta manera se utiliza en la
preparación de fertilizantes, como nitrato de amonio o sulfato de amonio.
Otro uso bastante frecuente es como producto de
limpieza; gracias a sus propiedades desengrasantes resulta de utilidad en la
remoción de manchas difíciles. Es usado diluido en agua.